アンモニウム (ammonium)は、化学式NH 4 の分子イオンである 。 アンモニア (NH 3)のプロトン化によって形成される。ページ 2 / 3 よぉ、桜木建二だ。化学の実験によく登場するフェノールフタレイン溶液って知っているか? 水溶液がアルカリ性かどうかを調べる目的で使用される試薬なんだが、なぜアルカリ性で変色するか知っている人は少ないかもしれないな。 アンモニア (化学式NH3)の性質まとめ 作り方 ①水酸化ナトリウム+塩化アンモニウム (+水) ②水酸化カルシウム+塩化アンモニウム (加熱) ③アンモニア水を加熱 集め方 上方置換法

化学基礎 弱酸 弱塩基の遊離反応はなぜ起こる 原理をわかりやすく徹底解説 化学の偏差値が10アップするブログ
アンモニア水 化学式 なぜ
アンモニア水 化学式 なぜ-下の反応式について質問なのですが、なぜ鉄イオンとアンモニア水 高校化学「水酸化アルミニウムの性質」 映像授業のTry ITこれを熱化学方程式であらわすと,次式のようになります。 HC l aq + NaOH aq = N aC l aq + H 2O + 56kJ "aq"は「アクア」と読み,多量の水を意味し, 化学式の後ろにつけると(薄い)水溶液を表



画像の3なのですが 硫酸銅 2 水溶液にアンモニア水を過剰に加えると Yahoo 知恵袋
「なぜアンモニアの噴水実験で色が変わったのかを説明しなさい。」 この課題によって、アンモニア水がアルカリ性を示すことを理解しているか確かめられる。 (科学的思考、実験観察の技能表現、知識理解) アンモニアの噴水実験の参考文献は多数あり。3次の中和反応を化学反応式で表し,生じた塩の名称を答えよ。 ただし,1:1は物質量の比を示す。この物質量比で反応させたときの化学反応式を書け。 (1)塩酸と水酸化ナトリウム (2)塩酸と水酸化カリウム (3)塩酸とアンモニア (4)硝酸と水酸化ナトリウム4 は2 価の酸,アンモニアNH 3 と水酸化ナトリウム NaOH はそれぞれ1 価の塩基である。吸収されたアンモニアの物 質量を 硫 ≈〔 mol〕とすると,次式が成り立つ。 ∴ ≈ = 38 * 103〔 mol/L〕 答 38 * 10 3 mol/L CHECK8 酸と アンモニ から生じた
あまり詳しく説明すると、ますます混乱してしまい本質的疑問から遠ざかる可能性がありますので、将来の課題としてある程度信じておくことを勧めます(「信じる者は救われる」という感じで申し訳けありません。 式中で「*印」は触媒上で活性化していることを表します。 H2 →2H* N2 →2N* H* + N* → NH* NH* + N* → NH2* NH2* + H* → NH3 (上記は素反 →酸化銀(ag 2 o)の暗褐色沈殿を生じるが、過剰のアンモニア水を加えると、銀イオンが錯イオンであるジアンミン銀(Ⅰ)イオンag(nh 3) 2 を形成して水に溶解し、透明な水溶液になります。 (反応式) ag 2 o4nh 3 h 2 o→2ag(nh 3) 2 2oh – ③ビーカーに②の溶液とグルコース(アセトアルデヒドアンモニア水アンモニアすいammonia water アンモニア NH 3 を 10W/V%の割合に水に溶かしたものと 日本薬局方 で規定されている。 アンモニア は 常温 では 気体 で,揮発性が強いので, 水溶液 はアンモニア臭があり,直接 かぐ と鼻 粘膜 を強く刺激する。 濃厚なアンモニアは強い局所刺激作用を有するが,本溶液程度の濃度のものを短時間皮膚や粘膜に接触させると
なお、水溶液中では、水 h 2 o が配位しているのが当然であるから、アクア錯イオンなどを表記するときは、水 h 2 o を省略して反応式を書くことも多いです。次に、水 h 2 o 以外が配位している代表的な錯イオンを示します。 (i) 配位子がアンモニア nh 3 の 青色の水酸化銅の沈殿ができて、さらにアンモニアを加えると濃い青色のテトラアンミン銅 (II)イオン溶液ができます。 反応式は以下の通り CuSO4 + 2NH4OH → Cu (OH)2↓ + (NH4)2SO4 Cu (OH)2+4NH3→ Cu (NH3)42 + 2OH 参考URL: http//homepage2niftycom/organicchemistry/ino http//www3justnetnejp/~konan/waku/a 化学を勉強したことのある人であれば、アンモニアが弱塩基であることはご存知でしょう。 では、なぜアンモニアが弱塩基なのか? その理由を問われて、自信をもって回答できるでしょうか? そこで、アンモニアが弱塩基である理由を考えていきたいと




化学基礎 弱酸 弱塩基の遊離反応はなぜ起こる 原理をわかりやすく徹底解説 化学の偏差値が10アップするブログ




硫酸イオンと 硫酸の化学式はなぜ違うのですか 硫酸にはなぜhがつくのに 硫酸イ アンサーズ
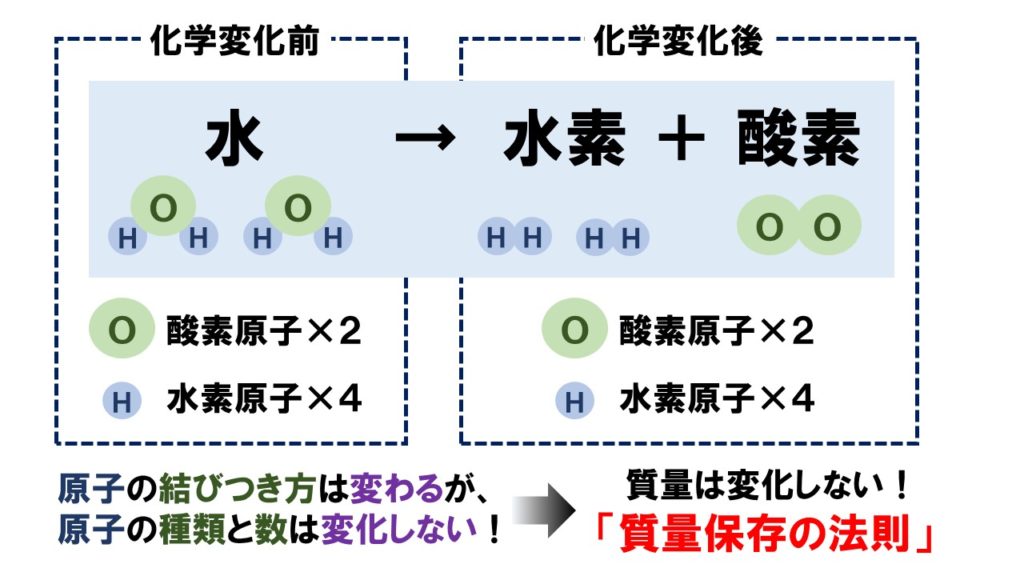
NH3 (アンモニア)H2O (水)=NH4OH (アンモニア水) まず、これが違う。 アンモニア水は、アンモニアが水に溶けているだけで、水と化合しているわけじゃない。 なので、 とは書かない。 食塩水を化学式で以下のように表さないのと同じ。 で、アンモニアは、水に溶けると一部が電離して、アンモニウムイオンと水酸化物イオンを生じる。 化学式で表すと、以下の通り アンモニウムイオンNH4はアンモニアが水に溶けた際の反応で発生します。 化学反応式:NH3+H2O→NH4+OH 水に溶かしたときに水分子から水素イオンをひとついただいています。 そしてNH4になっているのです。 水素分子は水素イオンをひとつ奪われOH(水酸化物イオン)になります。 アンモニア水はアルカリ性を示す理由です。 教科書を読んでみてください化学反応式の書き方 例1 水素の燃焼・・・水素+酸素→水 化学式・・・水素 (H2),酸素 (O2),水 (H2O) まず、水素+酸素→水をモデルと化学式で表す 両辺原子の数を数える 左辺のOが2個、右辺が1個なので右辺の水分子を増やす 右辺の物質は水なので、酸素
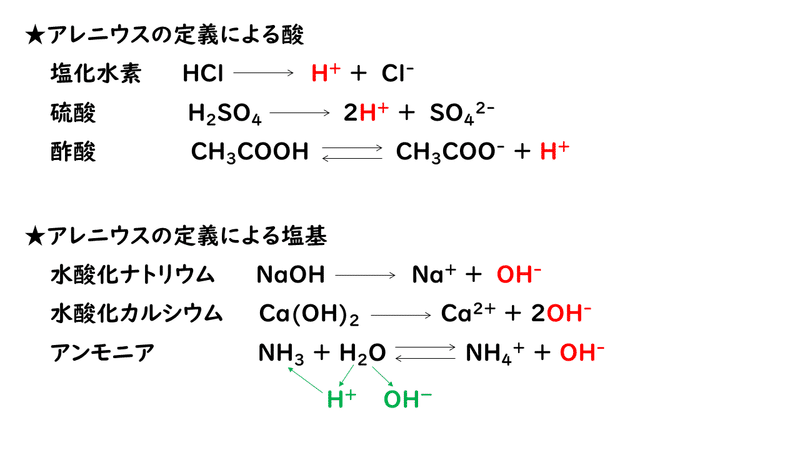



6 1 酸と塩基 おのれー Note




化学式について 水 H2 O h2o アンモニア n h3 h3n 原 Okwave
『アンモニア』『水』『メタン』『二酸化炭素』等です。 アンモニアは三角錐型 水は折れ線型 二酸化炭素は直線型 メタンは生四面体型 これらの分子の構造の理由は実は『 電子式 』を見ればわかるのです。その方法を見ていきましょう3 Mアンモニア水(NH 4OH)は市販のアンモニア水を5倍希釈して調整する. 操作 1)水酸化カルシウム飽和水溶液 5 mlを試験管(試験管Aとする)に入れ,1 ml駒込ピ ペットで05 Mリン酸2~3滴加える.沈殿が生成したらさらに05 Mリン酸を少しずつアンモニア水28% (NH 3) 和別名1 (水酸化アンモニウム) 和別名6 アンモニアスイ CAS RN ® メーカー名 キシダ化学




アンモニアの分子式は Nh ですが アンモニウムイオンのイオン式は Nh アンサーズ




アンモニアはなぜアルカリ性を示すのか アンモニアの特徴とともにわかりやすく解説 ジグザグ科学 Com
アンモニア水 (Aqua ammonia) (aqeuous ammonia) 別名 水酸化アンモニム (Ammonium hydroxide) 濃度又は濃度範囲 100% 分子式 (分子量) NH4OH (351) 化学特性 (示性式又は構造式) CAS番号硫化アンモニウム (りゅうかアンモニウム、ammonium sulfide)は 化学式 (NH 4) 2 S で表される アンモニア の 硫化物 である。 無色の 液体 、 水 に易溶 。 エタノール に可溶 。 ジエチルエーテル に不溶 。 硫化アンモニウム 英 ammonium sulfide (NH 4) 2 S 式量6814アンモニアが水に溶けるときは、 nh 3 h 2 o ⇄ nh 4 oh – という反応が進み、oh – を発生させるのでアンモニア水はアルカリ性を示す



実験13 アンモニアの噴水 1年理科 化学 Takaの授業記録12



Qck0d2a9as2853cudbqy0lc6cfz4a0e7e Xyz Kiso Electronically
水の化学反応式の作り方を説明しますね。 ①〈水→水素+酸素〉 反応前の物質名を左側に、反応後の物質名を右側に書く。 ②〈h₂o→h₂+o₂〉 それぞれの物質を化学式で表す。 ③〈h₂o h₂o→h₂+o₂〉 oの数を等しくするため、左側にh₂oを一個増やす。アンモニア水(水酸化アンモニウム)とは アンモニア水(水酸化アンモニウム)の化学的な性質や特徴、主な用途、使用上の注意などをご紹介します。 アンモニア水の原料であるアンモニアは、常温常圧では無色の気体として存在します。 悪臭防止法に基づく「特定悪臭物質」のひとつで、毒物および劇物取締法でも劇物に指定されています。 トイレの臭いの元 さらに、アンモニアは簡易的なクリーニング溶剤としても活躍します。特に水洗いが難しい衣類の洗濯には重宝しますので、その効果を知っておきましょう。 <アンモニア水の主な特徴> 化学名 アンモニア水(水酸化アンモニウム) 化学式 nh4oh 特徴




この問題で 煮沸して硫化水素を除き 冷却後濃硝酸を滴下したあと アンモニア水を加える Clear




50 グレア ナトリウム 水 反応 100 イラスト
アンモニア水の化学式(イオン式?)を教えてください。現在中学 アンモニアの化学反応式 N23H3→2NH3なぜこうなるかが アンモニアの化学反応式 化学のQ&A 解決済みOKWAVE 水と空気からアンモニア 100年続く製法超えられるか:朝日新聞 中1 理科 化学
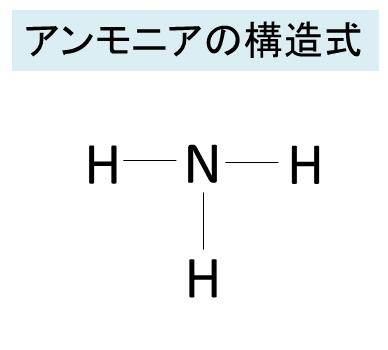



アンモニアの化学式 分子式 構造式 電子式 イオン式 分子量は イオン反応式は
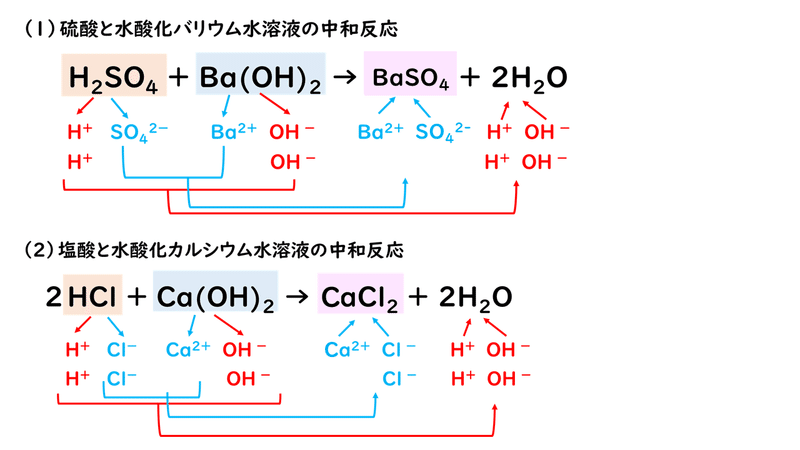



6 4 塩とその性質 おのれー Note
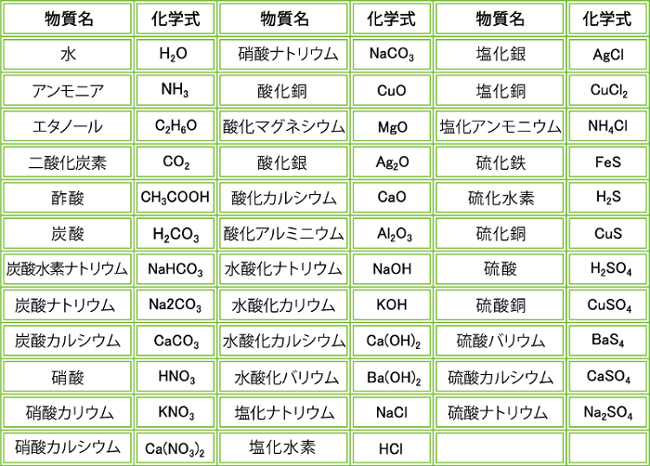



難易度が格段に上がる 中2理科 理論の1分野 暗記の2分野
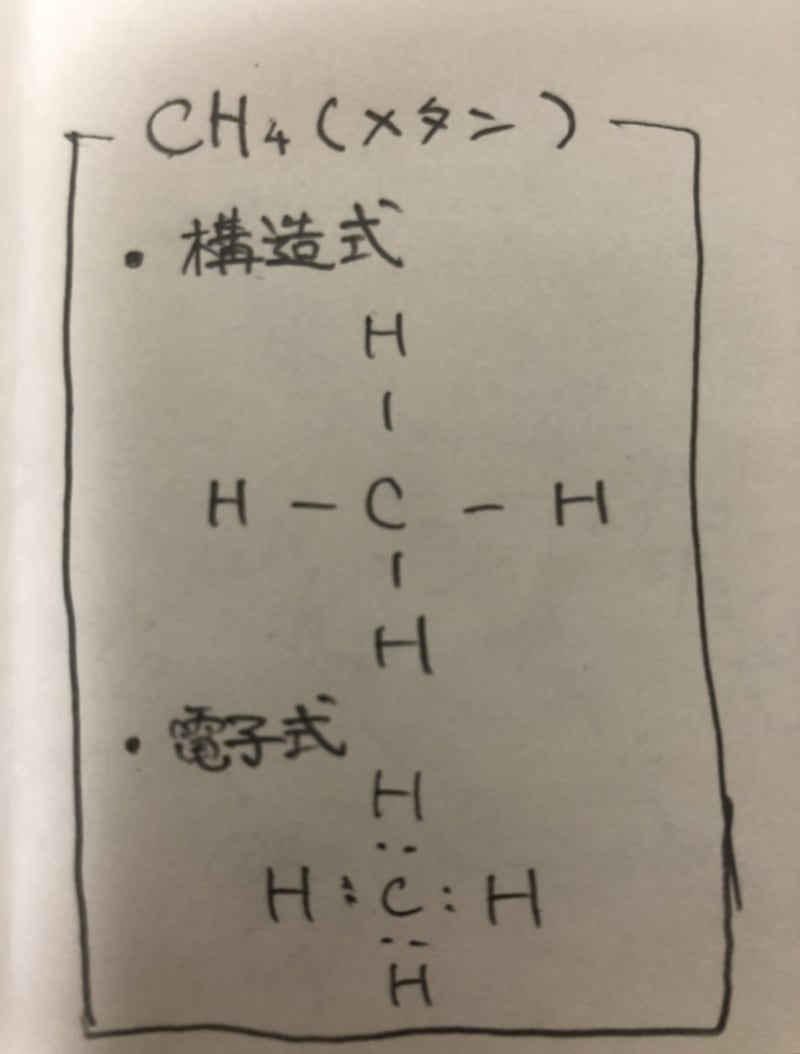



Ch4 メタン の構造式と電子式教えてください アンサーズ




理科 なぜ二酸化炭素が酸性 アンモニアがアルカリ性か なるほどの素
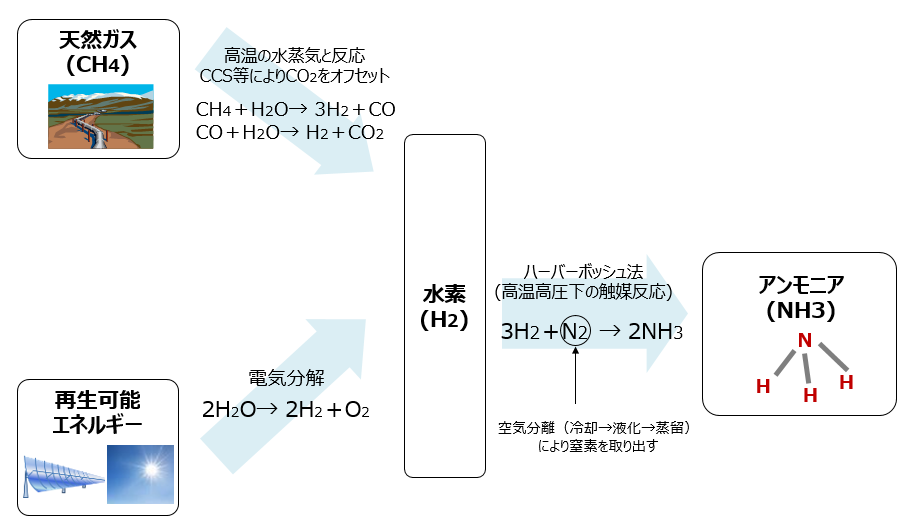



アンモニアが 燃料 になる 前編 身近だけど実は知らないアンモニアの利用先 スペシャルコンテンツ 資源エネルギー庁




170 00 Moll 0l00 Descubre Como Resolverlo En Qanda




なぜzn2 ではなくfe2 が沈殿したのでしょうか アンモニア水で沈殿す 化学 教えて Goo




銀が溶けた溶液に少量のアンモニア水を加えた時のイオン反応式をかけ 化学 教えて Goo



2



命運 日本が アンモニア に賭ける理由
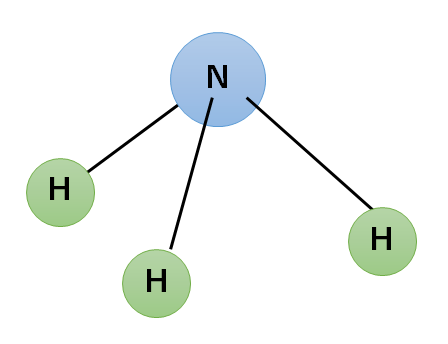



中3化学 アンモニアの利用 中学理科 ポイントまとめと整理



化学基礎107 2 電離度 アンモニアがアンモニウムイオン Yahoo 知恵袋




どうしてアンモニアの価数は3では無いのですか Clear



Qck0d2a9as2853cudbqy0lc6cfz4a0e7e Xyz Inorganic How To Make Nh3




中1理科 アンモニアの作り方 集め方 映像授業のtry It トライイット




汚れとお掃除の百科事典 ナチュラルクリーニング アンモニア水 サニクリーン



水素結合についての質問なのですが フッ化水素 水 アンモニアがこういう Yahoo 知恵袋




アンモニア水の電離式を写真のように誤解しています どうして紫下線のような式になるか教 Clear




アンモニアの化学式 分子式 構造式 電子式 イオン式 分子量は イオン反応式は




アンモニア水溶液には電離の際 H2oが付いているのに 酢酸水溶液についてないのは何故 Clear




なぜ中和で水を生じない場合があるのですか Clear




アンモニアの実験で 丸底フラスコに水が吹き上がった理由は 水にとけて 丸底フラスコ内 Clear




水素社会 はなぜ問題か 究極のエネルギーの現実 岩波ブックレット 小澤 祥司 本 通販 Amazon




中2理科 化学変化と温度変化 練習編2 映像授業のtry It トライイット



3




授業に潜入 おもしろ学問 自然科学科目群 化学 化学概論 I 中村敏浩 教授 京都大学広報誌 紅萠




化学反応式 中学生の学習法 Shun Ei Note




この問題 答えが4なのはわかるのですが なぜそうなるかがわかりません 解説をして アンサーズ
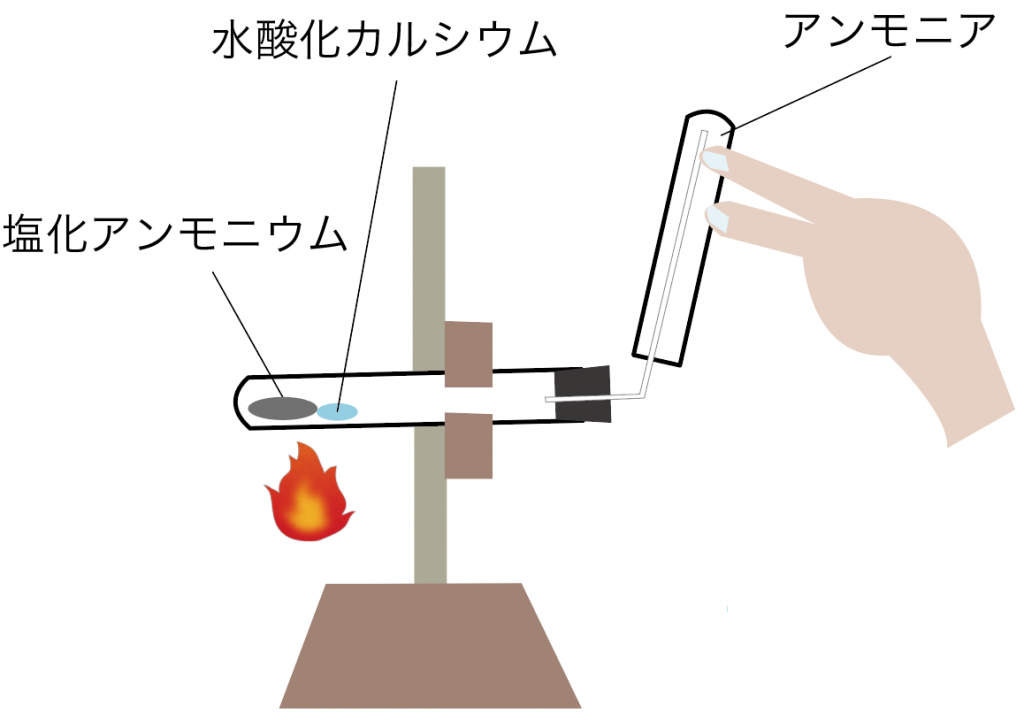



中1理科 3分でわかる アンモニアの発生方法 作り方 集め方 性質 Qikeru 学びを楽しくわかりやすく



錯イオン形成反応 受験メモ




Lihat Cara Penyelesaian Di Qanda



アンモニアの電子式はなぜhが下に来ないといけないのですか Yahoo 知恵袋
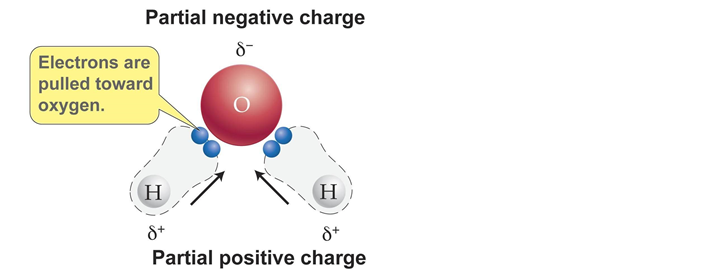



6月24 26日学習ログ アンモニアと塩化水素はなぜ水によく溶けるのか 翻訳のアシオト



Qck0d2a9as2853cudbqy0lc6cfz4a0e7e Xyz Kiso Composition Formula Molecular Formular



Qck0d2a9as2853cudbqy0lc6cfz4a0e7e Xyz Kiso Molecular Formular




Bar K Barsquare 5 67 Lihat Cara Penyelesaian Di Qanda




電離式の一覧 中学生用
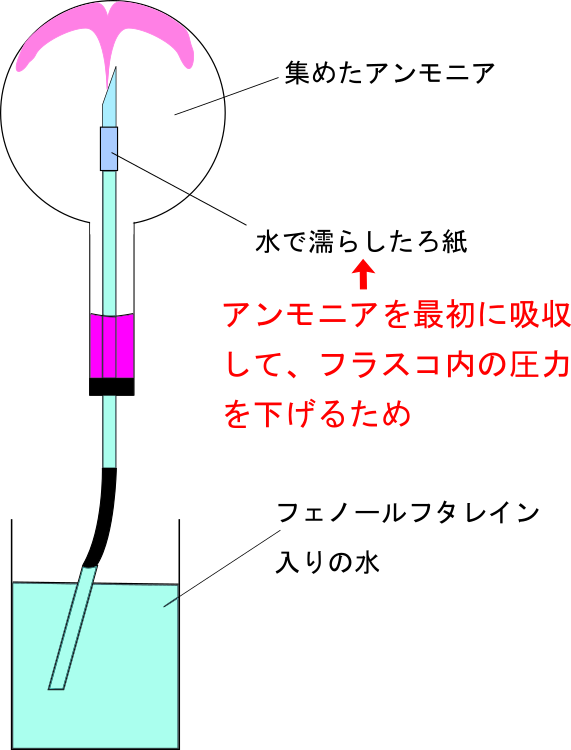



アンモニアの性質を利用して 赤色の噴水作り 理科の授業をふりかえる
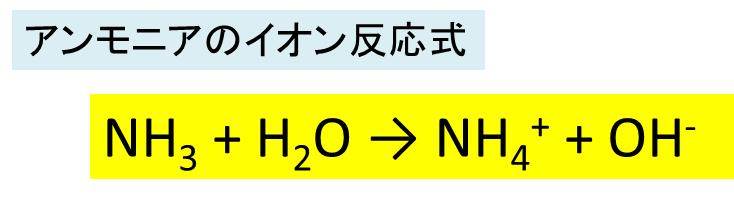



アンモニアの化学式 分子式 構造式 電子式 イオン式 分子量は イオン反応式は



中2理科 質量保存の法則のポイント Examee




アンモニア水とテトラアンミン亜鉛 の化学式についてですが なぜアンモニアは4mo Clear
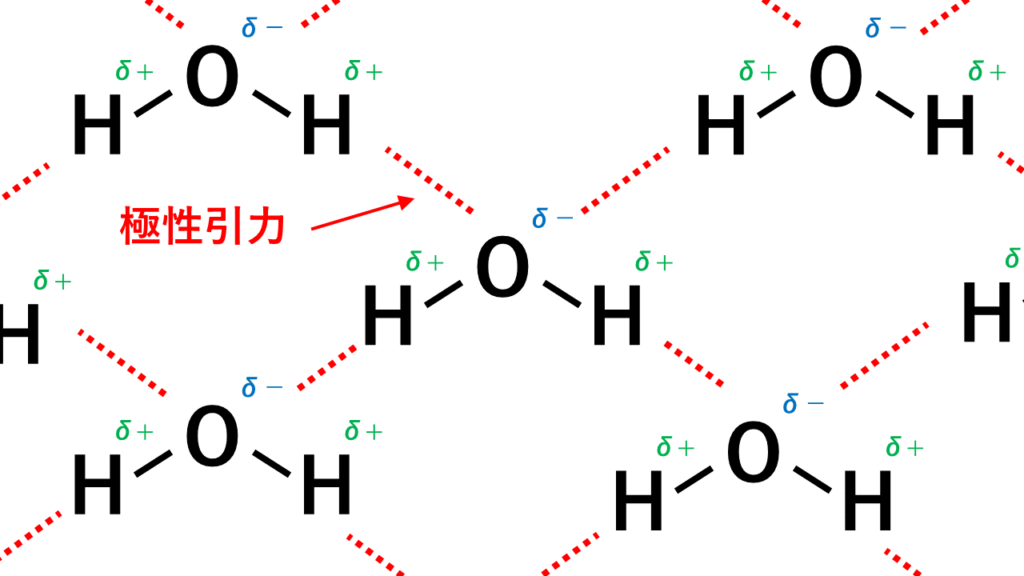



5分でわかる 水素結合とは フッ化水素 水 アンモニアの強さと沸点の順番が違う理由まで サイエンスストック 高校化学をアニメーションで理解する




イオン式 電離式まとめ 中学理科 ポイントまとめと整理



画像の3なのですが 硫酸銅 2 水溶液にアンモニア水を過剰に加えると Yahoo 知恵袋
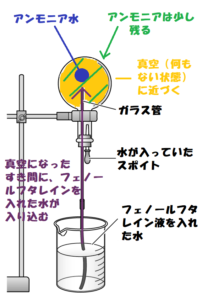



アンモニアの性質まとめ 中学生用



純水や超純水のph測定が難しい理由 M Hub エムハブ




族陽イオンの系統分析について 画像中で 青くマーカーされている化合物は Okwave



授業に潜入 おもしろ学問 自然科学科目群 化学 化学概論 I 中村敏浩 教授 京都大学広報誌 紅萠



化学です 写真の問題でアンモニア水を加えた時になぜアルミニウムだけが沈殿 Yahoo 知恵袋




Bar K Barsquare 5 67 Lihat Cara Penyelesaian Di Qanda




ドライアイスは化学式でいうと何ですか 氷はなぜ化合物なんですか 黒鉛 アンサーズ



アンモニアの電離式ってなぜh2oを足すのでしょうか Yahoo 知恵袋




炭酸水素ナトリウムはなぜアルカリ性を示すのか 反応式を使ってわかりやすく解説 ジグザグ科学 Com



実験13 アンモニアの噴水 1年理科 化学 Takaの授業記録12



1




5分でわかる フェノールフタレイン アルカリ性になると変色するのはなぜ 元研究員がわかりやすく解説 ページ 2 3 Study Z ドラゴン桜と学ぶwebマガジン



実験2で なぜ 水酸化バリウムと塩化アンモニウムを混ざらないようにビーカーに入 Yahoo 知恵袋



Q Tbn And9gctkhp4rlmsoxkfyjsrqfb80cfxiq3lawodl1p3tksvewza8m2vq Usqp Cau




中学3年の理科 動画 水溶液の酸性 アルカリ性の問題 Btb溶液とリトマス紙 19ch




授業に潜入 おもしろ学問 自然科学科目群 化学 化学概論 I 中村敏浩 教授 京都大学広報誌 紅萠




完全版 入試に出るアンモニアの製法をまとめたった 化学受験テクニック塾




なぜクエン酸は酸性で 重曹はアルカリ性なのか 両者の意外な関係とは 日本霜降社
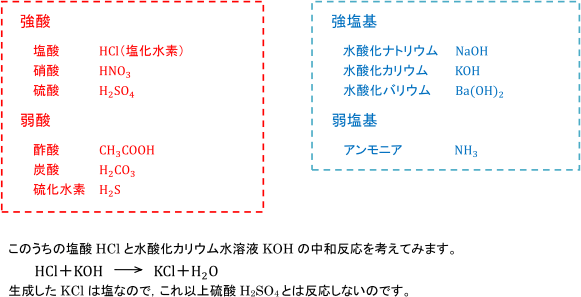



中和反応と塩 塩化カリウムと硫酸が反応しないのはなぜですか 化学基礎 定期テスト対策サイト




酸化銅の化学式 2種類の酸化銅を攻略する




電子対の数から考える分子の形 Vseprモデル




どうしてアンモニアだけ水を入れるんですか Clear
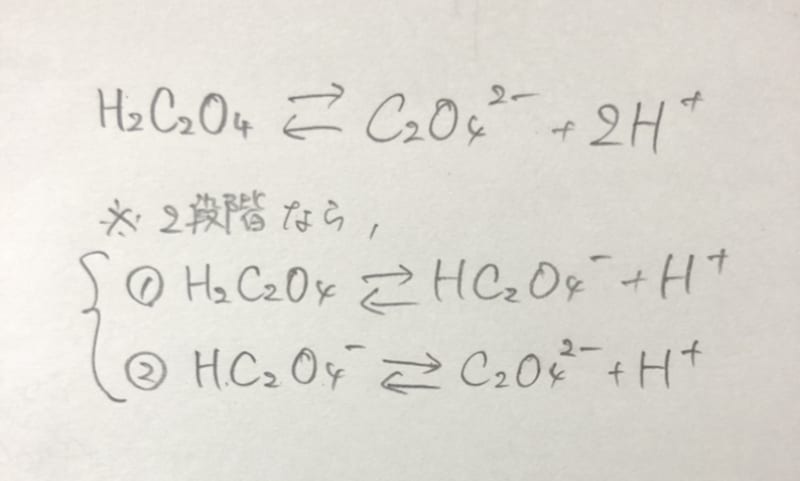



シュウ酸の電離式を教えてください アンサーズ




下の方のnh3 H2o が分かりません なぜアンモニアと水を足すんですか 化学 教えて Goo
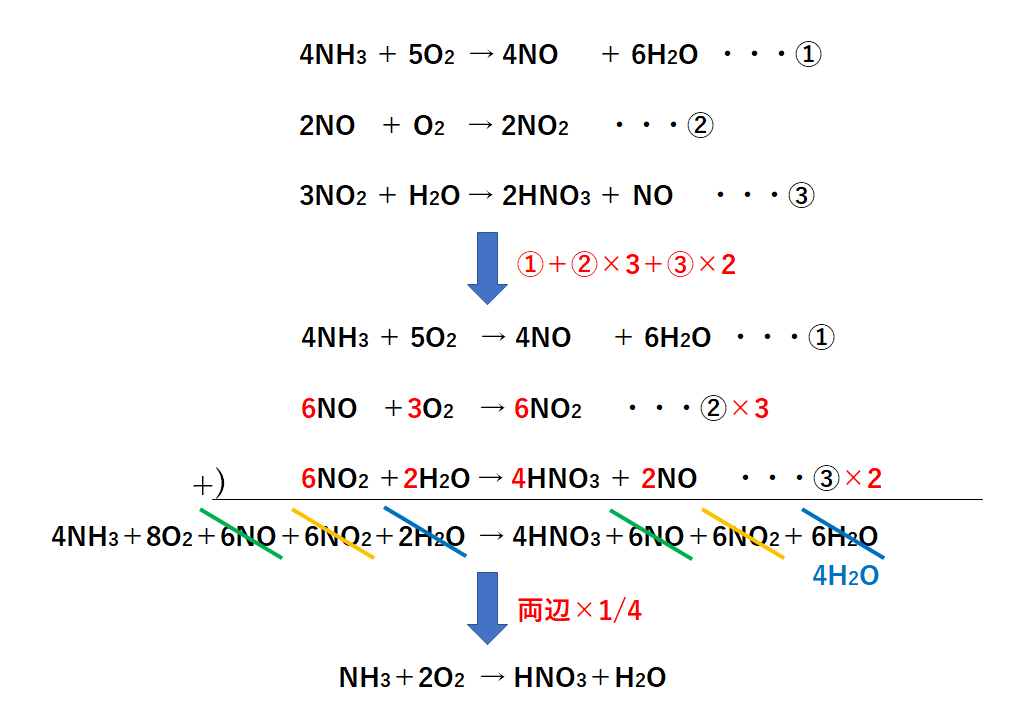



中3化学 アンモニアの利用 中学理科 ポイントまとめと整理




アンモニアはなぜアルカリ性を示すのか アンモニアの特徴とともにわかりやすく解説 ジグザグ科学 Com



下の反応式について質問なのですが なぜ鉄イオンとアンモニア水 Yahoo 知恵袋




アンモニアの赤い噴水 らくらく理科教室
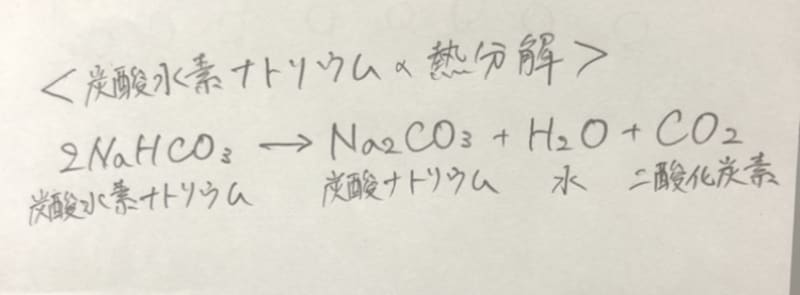



炭酸水素ナトリウムの化学反応式を教えてください アンサーズ
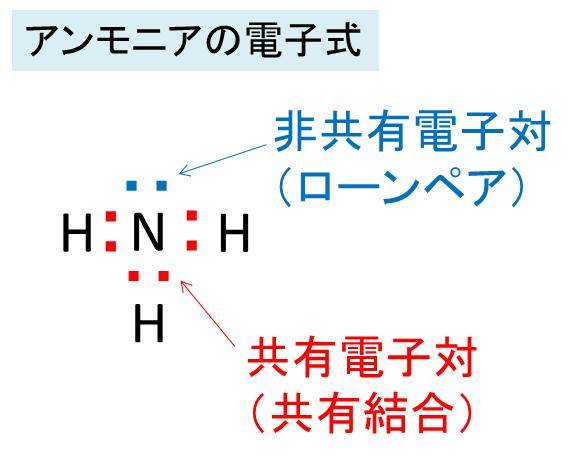



アンモニアの化学式 分子式 構造式 電子式 イオン式 分子量は イオン反応式は




1 A A 2 Descubre Como Resolverlo En Qanda




沖縄県名護市立名護中学校 理科 酸 アルカリと塩 化学変化とイオン 松田 晋介教諭
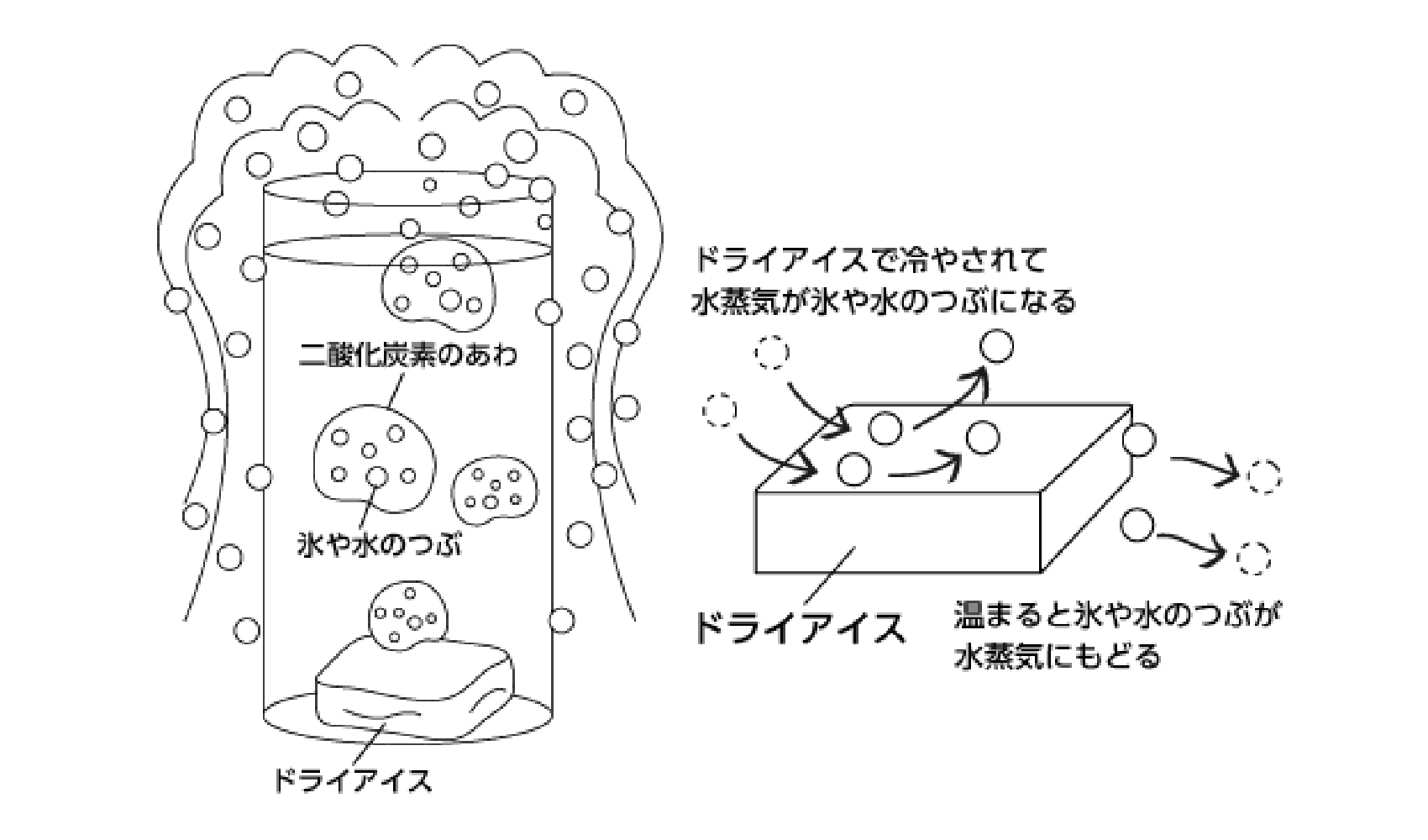



ドライアイスを水に入れるとどうしてけむりがでるの 理科の実験 科学なぜなぜ110番 科学 学研キッズネット
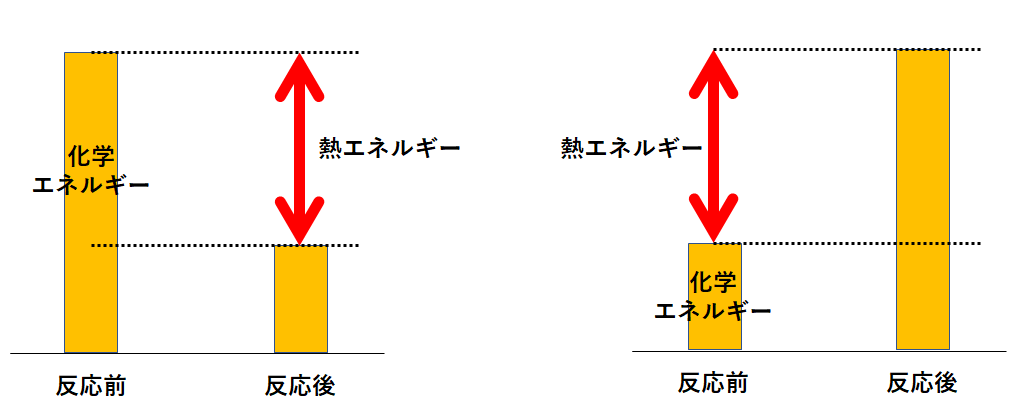



中2化学 発熱反応 吸熱反応 中学理科 ポイントまとめと整理
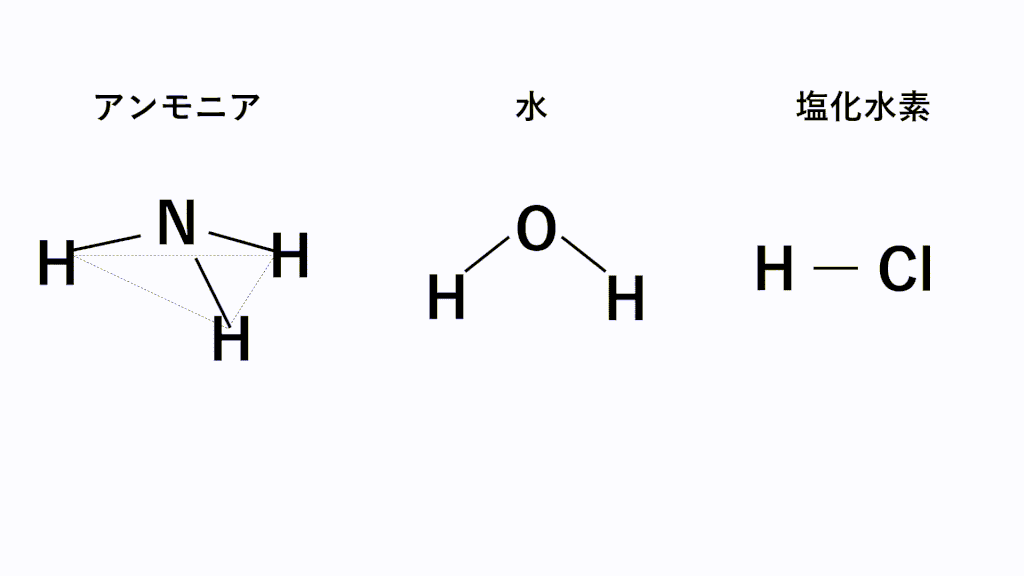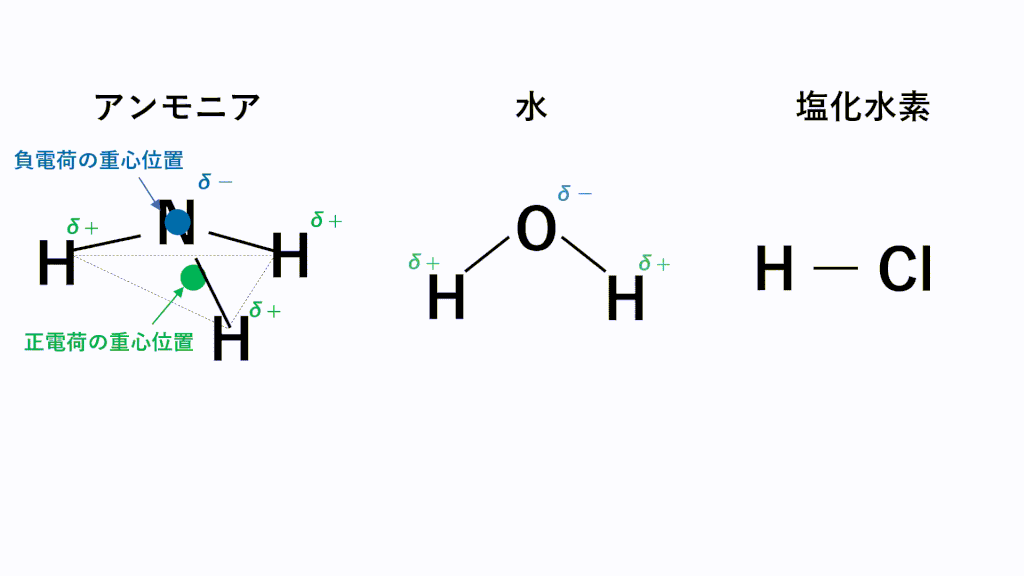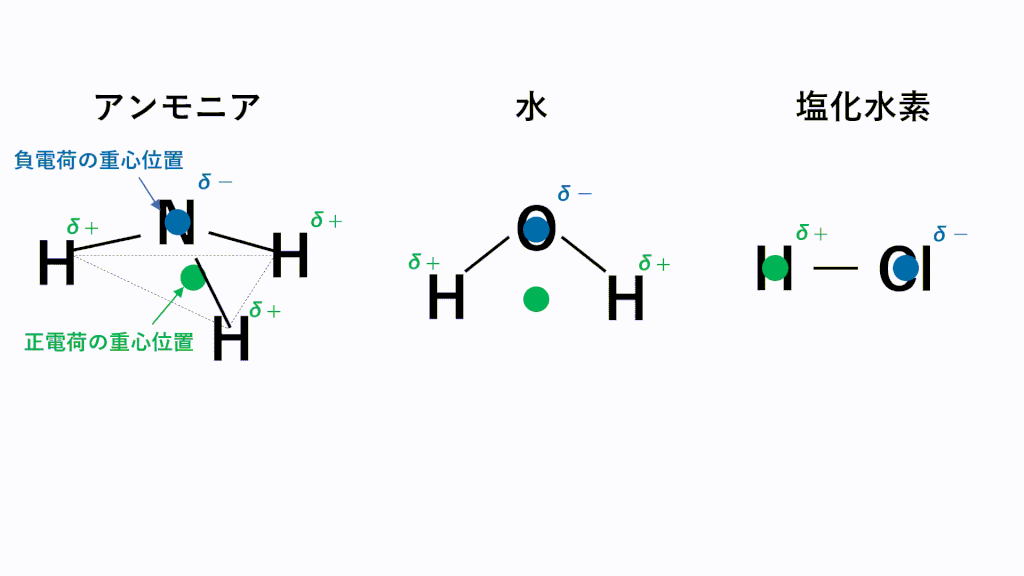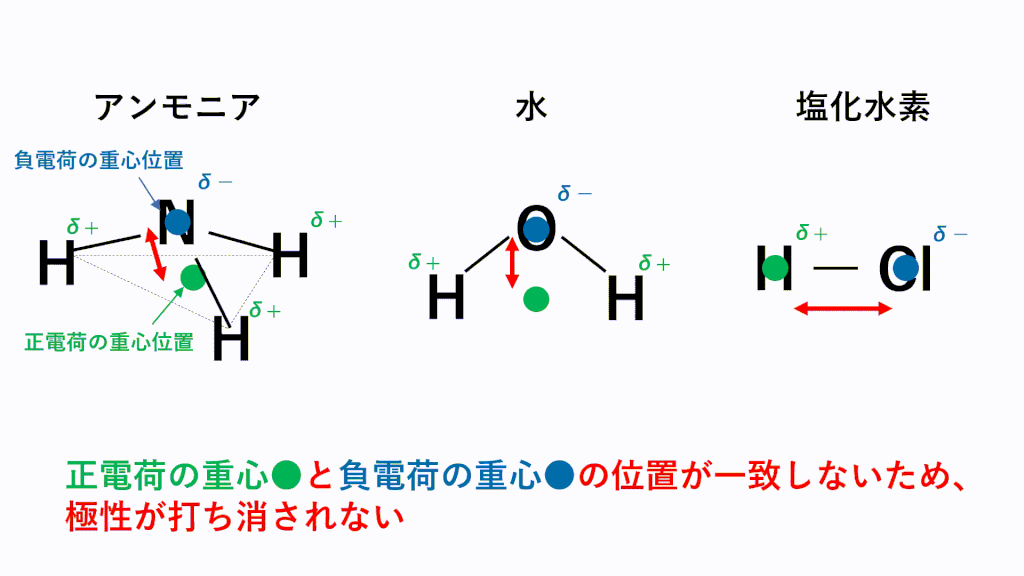



完全版 極性分子と無極性分子の考え方 分子の形と一覧をアニメーションで完全解説 サイエンスストック 高校化学をアニメーションで理解する




6 1 酸と塩基 おのれー Note



美しい 化学式 アンモニア Minecraftの最高のアイデア



Http Park Itc U Tokyo Ac Jp Nishiba Up Files Interview01 Pdf
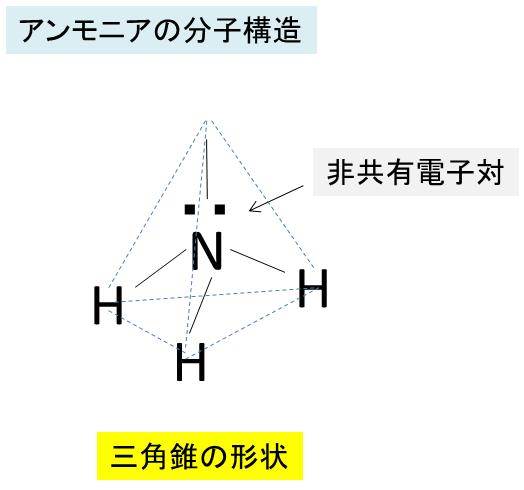



アンモニアが水に溶けやすい理由は
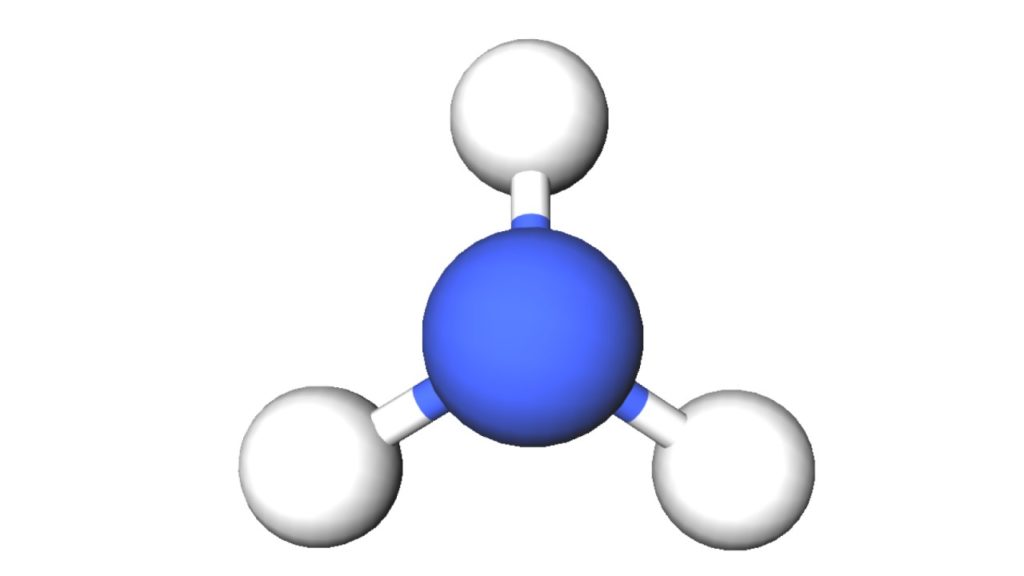



アンモニアはなぜアルカリ性を示すのか アンモニアの特徴とともにわかりやすく解説 ジグザグ科学 Com




5 2 化学反応の量的関係 1 おのれー Note



Http Www Keins City Kawasaki Jp 9 Ke9104 Jikken 30 Pdf




化学式 立体構造 Vsepr理論について 1 Youtube




高校化学 水酸化亜鉛の反応 映像授業のtry It トライイット



錯イオン形成反応 受験メモ




質問です Clear



Q Tbn And9gct Jpl5gztaqgcbkqjnbkrn3j Ydmqc Mdsqsxhwumi5lkbzz0 Usqp Cau
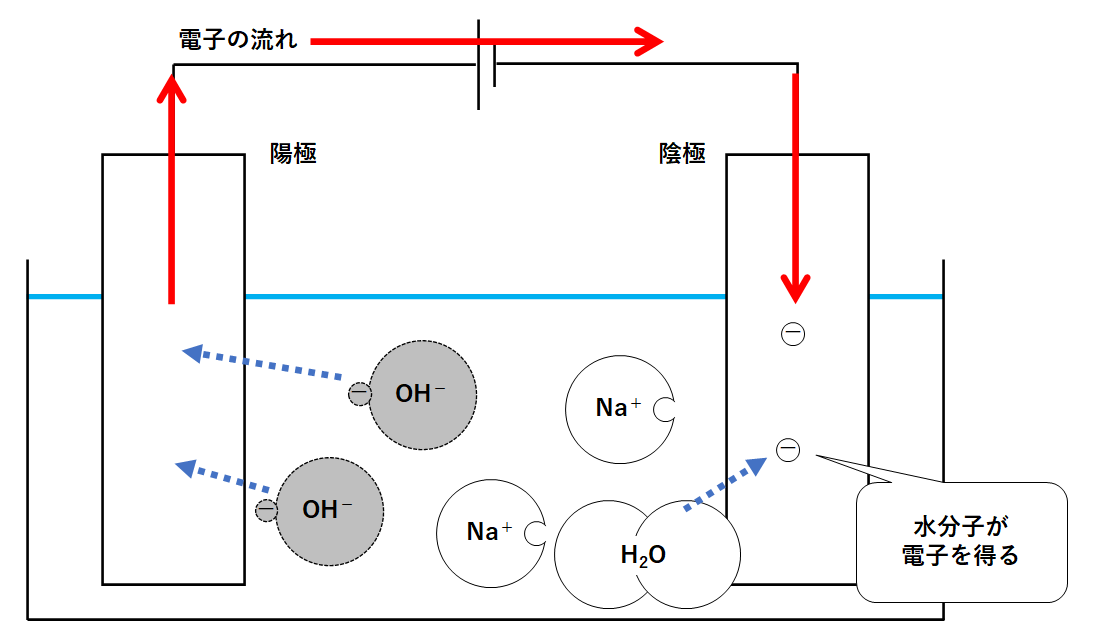



中3化学 水の電気分解 中学理科 ポイントまとめと整理




中学3年の理科 動画 水溶液の酸性 アルカリ性の問題 Btb溶液とリトマス紙 19ch



0 件のコメント:
コメントを投稿